喘息の病態
喘息の病態の基盤には 気道の慢性炎症が存在しますが その慢性炎症は 以下に説明する機序により起こってきます <2型炎症 2型免疫反応> 喘息の多くは 2型免疫反応とよばれる反応で起こり その反応には Th2リンパ球 2型自然リンパ球などが関与します @Th2リンパ球 Th2リンパ球は IL-4 IL-5 IL-13を産生しますIL-4 IL-13は B細胞からのアレルゲン特異的IgE抗体の産生を促し アトピー型喘息の病態に関与します IL-5は 喘息の病態に関与する好酸球の 分化・成熟・活性化を誘導します
また これらのサイトカインは 受容体を一部共有し 平滑筋増生 気道での粘液産生 杯細胞化生の誘導により 気道のリモデリング 呼吸機能低下を引き起こして 喘息の病態を形成します @ILC2・2型自然リンパ球 自然リンパ球のILC2は 通常は肺内には少数しか存在しませんが 喘息で増加し Th2リンパ球より大量のIL-5 IL-13を産生して 病態形成に深く関わります
喘息の引き金になると考えられる 感染やプロテアーゼ活性で誘導される組織傷害では 上皮細胞が産生するIL-33が ILC2を増殖させて IL-5 IL-13の分泌を促進します 上皮細胞は IL-25 TSLPも産生・分泌して これらによっても ILC2の増殖・活性化 IL-5 IL-13産生が増強されます TSLPは ILC2以外にも 好酸球 マスト細胞 樹状細胞も活性化し ILC2のステロイド抵抗性獲得にも関与します <非2型免疫反応> 非2型免疫反応が関与する喘息では 血中 痰中の好酸球増加は認められず 代わりに喀痰中の好中球が増加して 好中球性の炎症が認められます 一方 *Th17リンパ球 *ILC3 それぞれが産生するIL-17が 気道上皮に作用して IL-8が産生され好中球が集積されます
ILC3は IL-23 IL-1βにより活性化され IL-17を産生します 非2型免疫反応が関与するタイプは 重症喘息でも しばしばみられます 喘息には多様性があると説明しましたが 上記のような *特異的IgE抗体感作を示すアトピー型 *好酸球増加を示す型 *好中球増加を示す型 などが存在し こうした さまざまな機序により生じる慢性炎症により 気道に変化が生じて気流が制限され 気道の過敏性も誘発されます
<気道の慢性炎症が 気流制限を誘導する> 気道で炎症が起こると 次のような現象が起こってきます @気道平滑筋が収縮する
炎症細胞から分泌された ヒスタミン PGD2 ロイコトリエンC4/D4/E4などの作用により 気道平滑筋の収縮が起こります
これらの因子は さまざまな制御により発現が調節される 病態に関与する現場の役者であり 気管支拡張薬のターゲットになります 平滑筋の収縮は 冷気 煙 化学物質 気象変化 運動 心理ストレスなどでも起こり 迷走神経反射 アセチルコリン 神経ペプチドが関与します @気道が浮腫を起こす 炎症により各種の細胞から分泌された液性因子により 血管透過性が亢進し 気道粘膜が浮腫が起こります
@気道分泌が亢進する 気道での粘液の過分泌が起こると 気道内腔が狭小化するとともに 咳嗽 痰の原因にもなります
@気道のリモデリングが起こる 慢性炎症が長期化すると 気道のリモデリングが起きてきます
*気道上皮化の線維化 *平滑筋の肥厚 *杯細胞の過形成 などが起こってきて 非可逆的な気流制限 持続的な気道過敏性亢進をもたらし 難治化の原因になります <気道の慢性炎症は 気道過敏性も誘導する> 炎症の持続により *気道上皮の傷害 *気管支収縮を抑制する アセチルコリンM2受容体 βアドレナリン受容体の機能抑制 *気道平滑筋が収縮しやすいタイプに質的に変化する *線維化により気道壁のリモデリングが生ずる といった現象が起こり 気道抵抗が高まるとともに 過敏性がさらに誘導されてしまいます
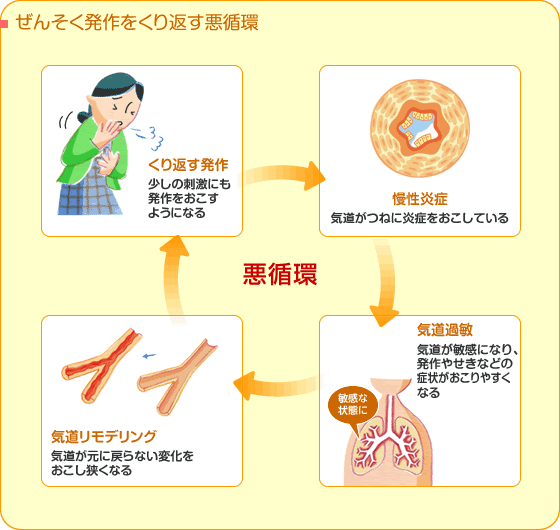
このように 喘息発作が繰り返し起こると 気道の慢性炎症→リモデリングが生じ これにより気道の過敏性がさらに高まり ちょっとした刺激で発作が起きやすくなり さらに炎症が積み重ねられていくという 悪循環が生じてしまうのです
高橋医院
























